約
尼氏症 (Johne's disease)
牛副結核桿菌症 (Map)(Paratuberculosis)
建盈(股)公司 陳銘政 DVM,MS
一、疾病名稱及原因
Johne's disease的英文發音為Yo-Knees,所以一般中文翻譯為「約尼氏症」。約尼氏症是在1905年,由具有獸醫師身分的德國細菌學家Heinrich A. Johne(圖1)發現本病是由一種禽結核分枝桿菌亞型的副結核桿菌(Mycobacterium Avium subsp. Paratuberculosis)所造成,這是一種基因研究顯示和禽結核分枝桿菌99%相似的抗酸性格蘭氏陽性菌,簡稱MAP,本疾病也稱為副結核桿菌症(Paratuberculosis)。
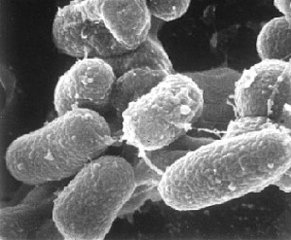
MAP(圖2)和造成人類結核病的人分枝結核桿菌(Mycobacterium tuberculosis),及造成牛或人類結核病的牛分枝結核桿菌(Mycobacterium bovis)是同類的細菌,但不同的是,MAP並不會造成人類或牛罹患結核病。
 |
 |
|
圖 1:德國細菌學家 |
圖 2: 電子顯微鏡下的牛副結核桿菌 |
約尼氏症是一種傳染性、慢性感染症,主要侵襲反芻類動物的小腸並造成肉芽腫性腸炎。牛感染後的特徵是反覆性、持續性下痢、體重逐漸降低、貧血、衰弱、消瘦和死亡。約尼氏症是世界動物衛生組織(OIE)極為重視的疾病。約尼氏症的病原體-副結核桿菌(Mycobacterium paratuberculosis)(MAP)會感染並造成反芻類動物(例如綿羊、山羊、美洲駝、鹿)、及圈養或自由放養的野生動物發病(例如野兔、狐狸、鼬鼠、鳥類)、在實驗中也會感染馬、犬及非人類的靈長類等雜食或肉食類動物(圖3)。
MAP能長期存活在土壤、水和糞肥環境中,對一般的消毒劑有抵抗力,但可被甲酚基酸(Cresylic acid)和鄰位苯基酚鈉(Na orthophenylphenol)等消毒劑殺滅。
約尼氏症分佈於全世界,台灣也不能倖免,根據家畜衛生試驗所最近抗體調查顯示約有9.0%乳牛牧場被汙染。在澳洲、挪威、冰島、日本、荷蘭、美國都已建立約尼氏症國家級防治計畫,目前除了挪威、瑞典和澳洲的某些區域已證實為非約尼氏症汙染國家或地區外,許多乳牛主要飼養國的正式文獻都指出,乳牛牧場的約尼氏症最高盛行率已達到20-25%。
約尼氏症對乳用或肉用山羊及綿羊產業,也都具有極大經濟威脅性。
 |
 |
二、傳播方式
受感染的動物會將MAP大量排放在糞便中,也會少量排放在初乳和牛乳中。MAP能抵抗惡劣環境並能在牧草地中存活1年以上,在水中存活的時間比土壤中還長。MAP通常藉由糞便經口傳染,所以糞便汙染的飼料、草料、飲水、墊料和乳房,以及在MAP汙染的環境中相互舔食,是牧場中散播MAP的主要途徑。向外購入MAP帶原牛隻,是牧場間散播MAP的重要原因。
6月齡以下的小牛最容易感染。年齡較大的牛比較有抵抗力,比較不會感染也比較不會發病。在其他動物方面,研究報告指出曾經從綿羊胎兒成功分離到副結核桿菌,其它報告也指出曾經從未曾飲用初乳的小羊血清中檢驗出副結核桿菌的抗體,這些報告似乎顯示若羊胎兒在子宮內感染MAP時,可能像成羊或年輕成羊發展出臨床症狀,但是目前還無法確認。牛也已證實可經由子宮感染,但不確知對後代有沒有影響,也就是還不知道懷孕母牛經由子宮感染MAP後,子宮內的胎兒會不會經由胎盤也感染(垂直感染)或發病。目前已知小牛最早在出生直後便會感染MAP,但由於病程發展緩慢,很少在2歲以下發病。年紀增加對本病的抵抗力也會增加,因此就算暴露於MAP中,成牛也很少受到感染。值得注意的是,使用帶原公牛自然交配時,也會經由汙染的精液傳染給健康的女(母)牛。
MAP經口攝食後,這種細胞內病原菌會被胃腸消化道尤其是小腸腸壁和相關淋巴結中的巨噬細胞吞噬。巨噬細胞原本是一種能夠吞噬並殺滅外來細菌的細胞。但是巨噬細胞並無法順利殺滅MAP,MAP會在巨噬細胞中增殖並造成巨噬細胞死亡。或許某些動物得以藉由細胞免疫反應增強巨噬細胞的殺菌能力而去除MVP感染,但其發生的機制尚待進一步了解。動物體對MVP這種細胞內寄生細菌的免疫反應會使腸壁外觀典型性變厚,也會在鏡檢時呈現扭曲的樣貌。
三、臨床症狀
約尼氏症在牛的主要特徵是呈現漸進性消瘦、消耗性、或惡病質臨床症狀的疾病,好發年齡為2-6歲,通常會在妊娠、分娩、寄生蟲感染、飼養管理失衡或運輸等緊迫誘因時發病(圖4)。罹病初期的症狀似有似無難以捉摸,只覺得體重減輕、產乳量下降或皮毛粗糙,對驅蟲劑、抗生素和殺菌劑治療通常沒有明顯反應。大多只會在疾病的惡化期呈現體重明顯下降和下痢的現象,但是就算如此,罹病牛在幾個月到幾年間仍看來健康,雖然體重一直減輕但是食慾正常,直到瀕臨死亡才失去食慾。
在牛會顯現持續性或間歇性的下痢或水痢便。其它反芻動物,例如綿羊和山羊不常見像牛一樣嚴重的水痢便,通常就算已經出現臨床症狀了,排便外觀還是很正常,但有時還是會出現間歇性下痢或軟便,有時出現糊狀便。有時可見精神不濟和間歇性輕度發燒。因此常被誤認為腸道寄生蟲感染、慢性創傷性胃炎、肝膿腫、球蟲感染症、腎盂腎炎、慢性營養不良、環境毒素和癌症,必須區別診斷。
典型的下痢便中不會含有血液、黏液或上皮細胞碎屑,也不會有裡急後重現象(即感覺急需大小便而無法順利排出之現象)。幾個星期或幾個月以後,下痢會變得更嚴重,體重開始減輕,皮毛或許粗糙,由於蛋白質流失性腸病緣故,可能發展出腹部和下顎水腫的水杓顎(bottle jaw)現象(即液體堆積在下顎處)(圖5),也造成血漿中總蛋白和白蛋白濃度降低。但γ-球蛋白濃度正常。
約尼氏症是一種漸進性的病程,病畜會在仍然機敏的情況下越來越瘦弱,體溫和食慾通常正常,但是經常口渴,最後病畜脫水、衰弱、嚴重惡病質而死亡。被感染的牧場,也許幾年內的死亡率都很低,但是非臨床性感染率可能高達50%,造成產能的巨大損失。
約尼氏症具有“冰山現象”,也就是牧場中只要有一頭牛出現臨床症狀,就表示另外還有5-15頭非臨床性感染牛存在。通常罹病牛中只有1%會呈現臨床症狀。(牛乳房炎的冰山現象為牧場中有一頭牛出現臨床性乳房炎,就表示另外還有40頭牛罹患非臨床性乳房炎)。
 |
 |
 |
|
圖 5:如圖片中箭頭所示-水杓顎 |
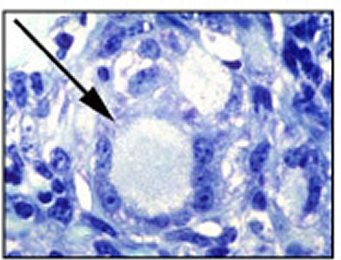
圖 6:如圖片中箭頭所示-巨噬細胞會融合 |
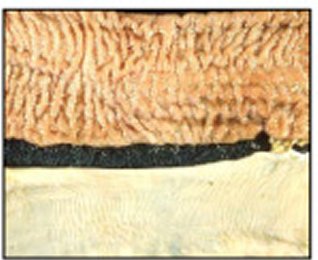
圖
7: MAP感染後,數以百萬計的淋巴
球和 |
四、病理變化
約尼氏症病原菌MAP的主要攻擊目標是下段小腸,也就是迴腸。迴腸壁中含有大量囊狀的淋巴樣組織,恰恰位於迴腸表面內側,稱為沛氏集合淋巴結(Peyer’s patches)。沛氏集合淋巴結中有系統聚集巨噬細胞和淋巴球,因此很像淋巴結。包圍沛氏集合淋巴結的上皮細胞稱為M細胞(Microfold cell)。這些具有特殊功能的獨特細胞能夠藉由內噬作用(Endocytosis),將腸管管腔中的有機體和抗原帶進細胞內部,或是藉由吞噬作用(Phagocytosis)將較大的固體顆粒,例如細菌,吞食進入細胞內部,再藉由穿胞運輸(Transcytosis)穿越上皮細胞屏障,而接觸沛氏集合淋巴結中的巨噬細胞和淋巴球(T細胞)等簡稱為APC的抗原呈現細胞(Antigen-Presenting Cells),這些APC都是免疫細胞,因此就刺激了黏膜免疫反應,動物體因而產生對抗環境中這些病原菌的保護力。
但MAP是非常特殊的細菌。當M細胞將MAP帶進沛氏集合淋巴結後,巨噬細胞會吞噬MAP並試圖消滅它,但卻原因不明的做不到。MAP反而在巨噬細胞中不斷增殖,最後殺死巨噬細胞,再擴散再感染附近的細胞。造成迴腸和其它組織的廣泛感染。
動物體的免疫系統對MAP侵入的反應是不斷招募並補給更多的巨噬細胞和淋巴球到感染部位。淋巴球會釋放出多種化學物質稱為細胞激素(cytokines),嘗試加強巨噬細胞的殺菌能力。巨噬細胞會融合形成大的細胞,稱為多核巨大細胞(multinucleated giant cells),企圖強化殺滅MAP的能力(圖6)。感染動物呈現多樣貌的病理學變化,通常數以百萬計的淋巴球和巨噬細胞在感染部位組織浸潤的結果導致腸壁明顯增厚,造成營養吸收不良和下痢(圖7),但是病理變化範圍從腸管完全缺乏肉眼病變到腸壁變厚變皺,鄰近淋巴結腫大和水樣化。通常病灶的嚴重程度和臨床症狀的表現沒有關聯。在病程拖久的末期,解剖中可發現瘦弱的病畜的心臟與腎臟已經沒有脂肪包圍。腸子的病灶或許輕微,但是末端小腸壁會出現典型瀰漫性增厚,黏膜雖然沒有潰瘍但會出現明顯的橫向皺摺。這些病灶有時會擴大並延伸到結腸與空腸。通常也會明顯出現漿膜淋巴管炎、以及腸繫膜淋巴結和其他局部淋巴結腫大現象。
在組織學上,呈現瀰漫性肉芽腫性腸炎,特徵是在腸道黏膜和黏膜下漸進性累積上皮樣巨噬細胞和多核巨大細胞。在巨噬細胞中有時可見稀少或大量的抗酸性細菌。通常病灶的嚴重程度和臨床症狀並沒有關聯。羊和鹿有時在腸壁和淋巴結會發展出鈣化、乾酪樣病灶。
隨後從血清中能夠檢驗出病畜對MAP感染的抗體,也表示病畜即將出現臨床症狀,也終將面臨死亡。
經濟動物中。羊是感染MAP並罹患約尼氏症後,病程較快較明顯的動物,就算給予足夠的食物,身體耗弱的症狀還是很明顯。一旦出現下痢症狀就表示已經到了疾病末期而會死亡。
五、診斷方法
市場上有許多商業化牛副結核桿菌檢測試劑。這些試劑或著重於檢測糞便或組織中的細菌(培養法、聚合?鏈鎖反應),或著重於尋求對於感染所產生的細胞免疫反應證據(皮內注射試驗、γ干擾素),或著重於檢測牛副結核桿菌抗原所誘導的抗體(酵素免疫分析法、洋菜膠免疫擴散法)。同時利用這些不同方法的試劑檢測,可以增加診斷的準確性。
解剖並對不同組織進行MAP細菌培養和組織病理學檢查是有如黃金般可靠的診斷。針對抗酸性細菌的組織樣品進行Ziehl-Neelsen染色,通常可以顯露出病灶中的大量分枝桿菌(Mycobacteria)。但是在某些病例,就算經過嚴謹的試驗也無法證明它們存在。從迴腸按壓塗抹所進行的傳統病理學抗酸性細菌染色法,是一種快速又便宜的初步診斷法(但是比較不準確)。珍貴具有價值的種畜,從迴腸和鄰近淋巴結活體切片後進行細菌培養和組織病理學檢查,能夠獲得最可靠的診斷。從許多組織都能夠分離到牛副結核桿菌,但是腸繫膜淋巴結、迴盲腸淋巴結、迴腸和肝臟是最被常分離到MAP的組織。
血清學檢查是在病畜存活時,快速又便宜的臨床診斷方法:對具有臨床症狀的罹病牛隻檢出靈敏度>85%:對不具臨床症狀的外觀正常牛隻,在感染後期並大量排菌時的檢出靈敏度∼45%。和血清學檢查比較,酵素免疫分析法(ELISA)的靈敏度及確診性較高,也比較適合使用於測定某牧場的感染盛行率。但是大量使用酵素免疫分析法以確定牧場中的牛隻應該淘汰或隔離,是一種昂貴的疾病控制方法。糞便培養法比血清學檢查更敏感也更確診,但是MAP長得很慢(2-4個月)費用也比較貴。將糞材樣品混合檢查(例如5個糞材混合成1個),能夠降低檢查費用,只是也會降低一點檢查的靈敏度。每個實驗是對本病菌的分離技術與熟練度大不相同。必須選擇經過認證的實驗室。
大部分得以感染羊隻的菌株並不會在固體培養基中生長,必須利用液體培養基。
某些實驗室也曾提出報告指出聚合?鏈鎖反應(PCR:polymerase chain reaction)的敏感度及確診性和糞便培養法差不多但比較快速:某些實驗室卻發現並非如此。費用高是PCR最主要的缺點。PCR和其他檢驗方法使用於牛都有效,並不代表使用於其他動物的糞材樣品也有效。
細胞免疫試驗,例如皮內約尼試驗(intradermal Johnin test)、淋巴細胞轉化試驗(lymphocyte transformation test)、和γ-干擾素(γ-interferon)大多僅被應用在研究上,對於末期的臨床病例可能呈現陰性反應。近來牛副結核桿菌的基因已被探索出來,可望做為開發新診斷方法的基礎。
靜脈約尼試驗(intravenous Johnin tests)、以及糞材染色鏡檢又稱為抗酸性染色法 ( Acid-Fast Stain)的齊耳-倪耳生二氏法(Ziehl-Neelsen Method),因為敏感度低且確診性不足而被淘汰。補體試驗(The complement fixation (CF) test)的準確度也比其他血清學檢查低。
六、治療和預防
本病沒有適當的治療方法,抗生素中只有 Amikacin 可減少患畜糞便中的菌體數,每天二次,每次 250 mg,須給予一個月之久,另外如鏈黴素及抗結核藥 ( INAH,Rifampin ) 等可改善臨床症狀但無法治癒,由於藥劑療法價錢昂貴所以不實用。預防上需要良好的衛生管理實務以避免年幼動物暴露於病原菌。小牛小羊出生的地方必須沒有糞便,一出生就立刻帶離母畜,瓶裝餵食經過巴斯德滅菌法處理的初乳,或者瓶裝餵食經證實本病陰性母牛的初乳,並盡可能與成牛隔離飼養直到1歲以上。初乳期以後必須使用小牛或小羊代奶粉而非廢棄生乳,除非這些生乳經過巴斯德滅菌法處理。
每年都要篩檢牛群或羊群一次或二次,以保持動物健康並遠離約尼氏症。
成牛例行健檢能夠協助並監控本病的防治效果-即牧場中一旦出現確診病例就全面檢測以確知盛行率。確認陽性時,尤其是大量排菌或以酵素免疫分析法(ELISA)檢驗呈現強陽性結果時應儘快撲殺。每年重複全面檢測乙次,直到盛行率降低(<5%)。由於可能發生子宮內感染,所以更進一步的防治策略是將呈現陽性反應或甚至已經發病的母牛所生的仔牛都撲殺。新購入的女牛必須確認來自沒有遭受本病汙染的牧場,入場前也必須檢驗合格。全面使用冷凍精液配種,避免向外購入公牛。
減少糞便汙染的措施也能降低本病的發生,例如提升採食槽和飲水槽的高度,或實施管線飲水替代水槽飲水,增加清除牛舍糞便的次數。畜主必須了解本病的控制措施,至少要五年才能見到成效。
約尼氏症感染牛群之血中磷、鈣、鈉、鉀和鎂不足時病情較嚴重,因此必須適度補充良好品質的維他命及礦物質。
七、菌苗的使用
約尼氏症的MAP菌苗配方隨著製造廠商不同而有不同,並且有許多國家要求MAP菌苗施打時,必須由審定合格的人員操作,也只能使用於嚴重感染的牧場。MAP菌苗意外注射到施打人員時,將會造成嚴重急性的組織壞死、慢性的滑膜炎和肌腱炎。
牛隻接種不活化全細胞的礦物油佐劑MAP菌苗,會在注射部位產生幾英吋直徑不等的肉芽腫,也可能對之後的結核菌素皮內注射試驗造成陽性反應,導致無法與肺結核之感染病例區別,所以許多國家並不使用MAP菌苗,而以撲殺發病牛、篩檢無症狀感染牛及防止進口帶原牛為清除方針。
1月齡以下的仔牛施打MAP菌苗能夠有效降低本病的發病率,但是無法避免牧場中產生新的感染病例,也無法避免病牛排菌。因此施打MAP菌苗外,還需要良好的管理和衛生。
西班牙的山羊在施打MAP菌苗後發現羊群的生產年限增加,澳洲也正在研究將MAP菌苗使用於綿羊的可行性。
八、本文後記
在臨床判斷並得知某些酪農的牧場遭受MAP汙染並出現「約尼氏症」臨床症狀,不禁為牛羊飼養產業耽心而投稿本文,並期望酪農與政府相關單位更重視MAP的防治,適時研擬並執行「約尼氏症」清除計畫。
我們不應該再將MAP感染的「約尼氏症」臨床症狀,誤以為是寄生蟲感染,就像我們也不應該忽視「牛呼吸道融合性病毒」(BRSV)對牛隻的危害,而一直單純判定為牛流行熱(BEF)。
備註:本文所有圖片具有版權,並感謝版權所有者"Johne's Information Center, School of Veterinary Medicine, University of Wisconsin-Madison, USA http://johnes.org"及Dr. Manning的使用授權及進一步的說明。
參考文獻
|
1. |
吳永惠。1991。 牛病學。164-168。 |
|
2. |
酪農天地。2009。乳協的產業服務功能。88期(6∼8)。 |
|
3. |
蔡向榮、呂榮修。1995。八十四年度重要牛病診斷與防治研討會-牛副結核病(Paratuberculosis)。中國畜牧雜誌第五十四冊合訂本1995年七月號至1995年十二月號第 27 卷 (95) 第 11 期 ( 91∼96 )。 |
|
4. |
高淑娟、呂完教、曾昭南、賴光明。牛副結核感染症(Bovine Paratuberculosis)。 |
|
5. |
陳銘政。2003。約尼氏症 (Johne's Disease)…您或許並未倖免?!。建酪知訊920116第18期。 |
|
6. |
Huang Chen-Shen。2009。The seroprevalence of paratuberculosis in Taiwan. |
|
7. |
Liying Lei, Brandon L. Plattner, and Jesse M. Hostetter。2008。Live Mycobacterium avium subsp. paratuberculosis and a Killed-Bacterium Vaccine Induce Distinct Subcutaneous Granulomas, with Unique Cellular and Cytokine Profiles。Clinical and Vaccine Immunology, May 2008, p. 783-793, Vol. 15, No. 5 |
|
8. |
William P. Shulaw, DVM, MS。Johne's Disease in Sheep and Goats。Ohio State University。Veterinary Preventive Medicine。VME-0003-01. |
|
9. |
Paratuberculosis.Net。Is the major cause of Functional Dyspepsia (FD), Irritable Bowel Syndrome (IBS) and Crohn's Disease (CD) Mycobacterium Avium subsp. Paratuberculosis (MAP) infection? |
|
10. |
Wikipedia。Mycobacterium avium subspecies paratuberculosis。 |
|
11. |
Ole Sorensen, Shirley Rawluk, John Wu, Ken Manninen, and Gerald Ollis。 |
|
Mycobacterium paratuberculosis in dairy herds in Alberta。Can Vet J. 2003 March; 44(3): 221–226. |
|
|
12. |
ParaTB pages。Does Mycobacterium paratuberculosis cause Crohn's disease。 |
|
first published:- Saturday, 15th March 1997. |
|
|
13. |
Paratuberculosis Johne’s disease OIE. |
|
14. |
The Merck Veterinary Manual。 2008。Paratuberculosis。 |